|
|||||||||||||||||||||||||||||||||
|
|
|
|
|
|
|||||||||||||||||||||||||||||
7.2.1 ELEKTROKEMIJSKI POTENCIALI |
|
||||||||||||||||||||||||||||||||
|
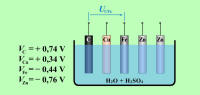
Če cinkovo ploščico potopimo v raztopino bakrovega sulfata (slika 7.2.1), bodo zaradi kemijske reakcije cinka z elektrolitom ioni cinka Zn++ začeli odhajati v elektrolit. Na ploščici bo začel nastajati presežek negativne elektrine, zato bo začela privlačiti pozitivne ione bakra Cu++ iz elektrolita in se obdajati z bakrom. |
|
||||||||||||||||||||||||||||||||
|
Ugotovljeno je, da je izmenjava elektrine med elektrodo in elektrolitom v splošnem neenakovredna. Zato zavzamejo kovine, ki z ioni oddajo elektrolitom več pozitivne elektrine, kot je dobijo iz elektrolita, proti elektrolitu negativni električni potencial in obratno. |
|||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||
|
Zaradi različnih izmenjav elektrin med kovinskimi elektrodami iz različnih snovi in elektrolitom, se razlikujejo tudi njihovi elektrokemijski potenciali. Kot primerjalni (izhodiščni) potencial 0 V je po dogovoru izbran elektrokemijski potencial vodikove elektrode. Po velikosti urejeni elektrokemijski potenciali tvorijo lestvico elektrokemijskih potencialov kovin (preglednica 7.1.1.1), ki jo po njenem utemeljitelju imenujemo tudi Voltova napetostna lestvica kovin. |
|||||||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||||||
|
Preglednica 7.2.1.1: Elektrokemijski potenciali |
|||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||
|
|
|||||||||||||||||||||||||||||||||
|
|